400-965-9800
发布时间:2026-04-20 14:06:52
2026最新进展全梳理(含IND/IIT 清单)
截至2026年4月,国内γδT细胞治疗已迈入IND获批提速、IIT研究全面铺开的关键阶段,实体瘤、血液肿瘤、自身免疫性疾病等多适应症布局初见成效。本篇将从细胞背景、作用机理、临床应用方向、国内最新临床进展四大维度,全方位解读γδT细胞治疗的研发与临床转化现状。
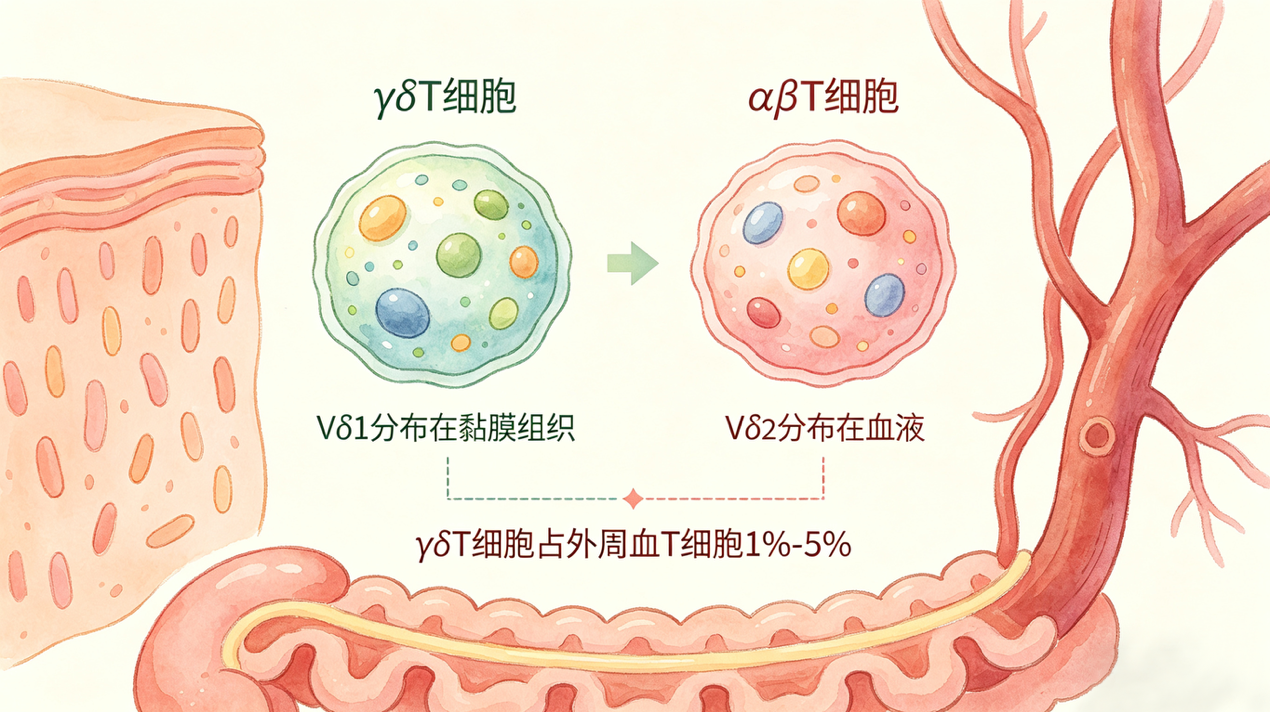
γδT细胞是T细胞家族中的特殊亚型,与我们熟知的αβT细胞(占外周血T细胞60%-70%)不同,其表面T细胞受体由γ链和δ链组成,而非传统的α链和β链,这也决定了它独特的生物学特性。
细胞分布与分型
γδT细胞在人体内含量极低,仅占外周血T细胞的1%-5%,主要分布于肠道、皮肤、黏膜等屏障组织,是机体抵御病原体、清除异常细胞的第一道防线。
根据δ链亚型不同,主要分为Vδ1 T细胞和Vδ2 T细胞:Vδ1 T细胞多存在于组织黏膜中,擅长浸润肿瘤组织;Vδ2 T细胞主要存在于外周血,是目前临床研究最广泛、产业化最成熟的亚型。
核心生物学优势
区别于传统免疫细胞,γδT细胞兼具先天免疫与适应性免疫双重特性,无需经过抗原呈递细胞致敏,即可快速启动免疫反应;同时具备异体输注无移植物抗宿主病(GvHD)、不受人类白细胞抗原(HLA)配型限制、可批量制备现货使用等优势,完美解决了传统CAR-T细胞个体化制备、成本高昂、周期长的痛点。
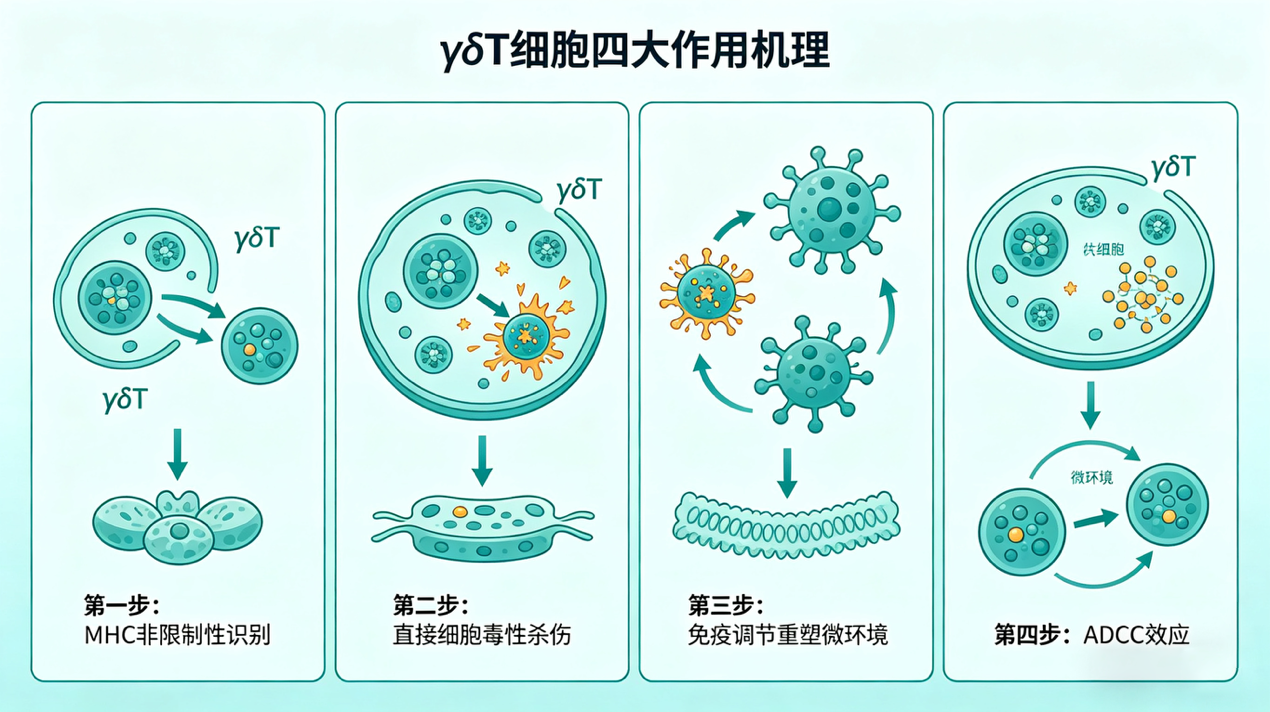
γδT细胞作用机理:多通路精准清除病灶
γδT细胞杀伤肿瘤细胞、调控免疫紊乱的机理,主要通过以下四大通路实现,作用机制清晰且高效,为临床治疗提供了坚实的理论基础:
1. MHC非限制性抗原识别
传统αβT细胞需通过MHC分子识别肿瘤抗原,而肿瘤细胞常通过下调MHC分子实现免疫逃逸。γδT细胞可直接识别肿瘤细胞表面的应激抗原、磷酸化抗原、异常糖基化分子,完全绕过MHC限制,精准识别并杀伤逃逸的肿瘤细胞。
2. 直接细胞毒性杀伤
γδT细胞可释放穿孔素、颗粒酶等细胞毒性物质,直接裂解肿瘤细胞;同时表达FasL,与肿瘤细胞表面的Fas结合,启动肿瘤细胞凋亡信号,诱导其程序性死亡,从根源上清除病灶。
3. 免疫调节与微环境重塑
γδT细胞能够分泌IFN-γ、TNF-α、IL-17等多种细胞因子,激活机体自身NK细胞、CD8+杀伤性T细胞等免疫细胞,形成协同抗肿瘤免疫网络;同时改善肿瘤免疫抑制微环境,抑制调节性T细胞(Treg)、肿瘤相关巨噬细胞(TAM)的免疫抑制作用,让免疫细胞重新发挥抗肿瘤效果。
4. 抗体依赖的细胞介导的细胞毒性作用(ADCC)
γδT细胞表面表达CD16等Fc受体,可结合肿瘤特异性抗体,靶向杀伤被抗体标记的肿瘤细胞,实现与抗体药物的联合治疗,大幅提升抗肿瘤疗效。
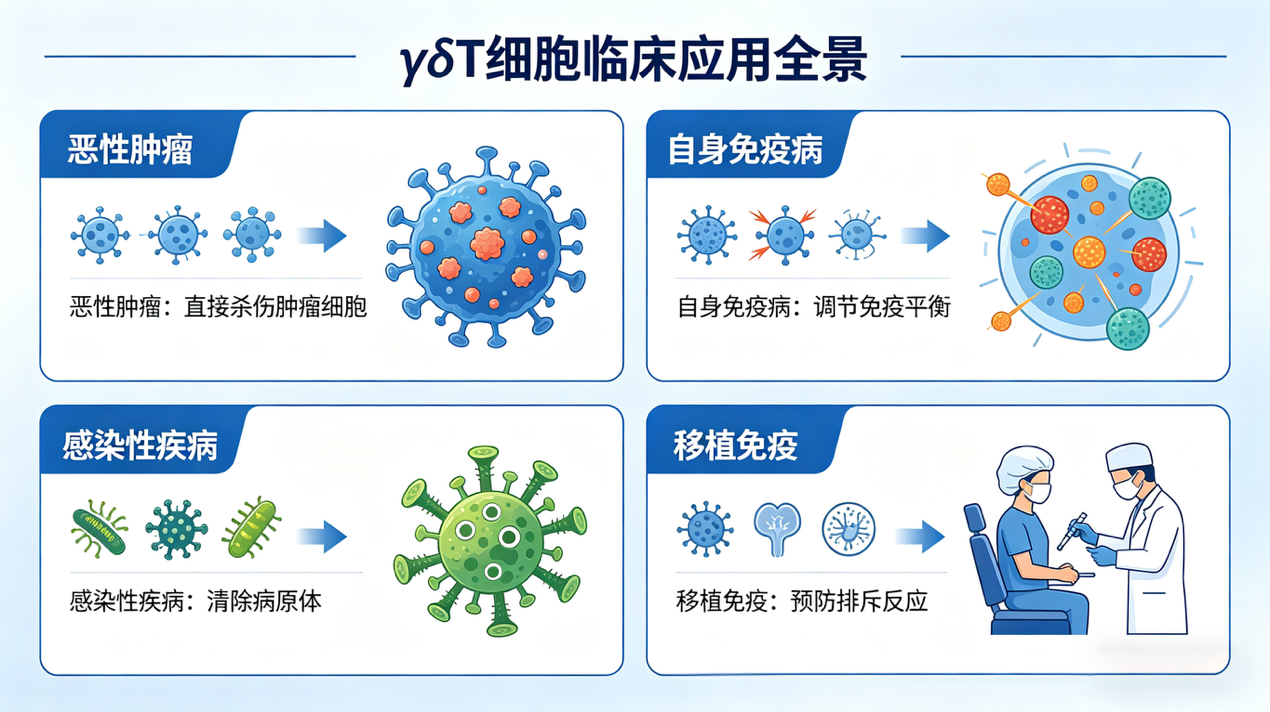
γδT细胞临床应用方向:全疾病领域覆盖,潜力无限
基于独特的作用机理,γδT细胞的临床应用场景极为广泛,涵盖恶性肿瘤、感染性疾病、自身免疫性疾病、移植后排异防控四大领域,其中恶性肿瘤是目前临床研究的核心方向。
一、恶性肿瘤:实体瘤+血液瘤双线突破
1. 实体瘤
实体瘤一直是细胞治疗的难点,而γδT细胞凭借强大的肿瘤浸润能力、免疫微环境重塑能力,在多种实体瘤治疗中展现出优异潜力,包括晚期肝细胞癌、中枢神经系统恶性肿瘤(脑胶质瘤)、膀胱癌、肺癌、黑色素瘤、胰腺癌、乳腺癌等,是目前国内临床研究的重点适应症。
2. 血液肿瘤
针对复发/难治性急性淋巴细胞白血病、急性髓系白血病、淋巴瘤、多发性骨髓瘤等血液肿瘤,γδT细胞可快速清除体内残留肿瘤细胞,降低复发风险,尤其适用于造血干细胞移植后复发防控。
二、其他疾病领域
1. 自身免疫性疾病
利用γδT细胞的免疫调节功能,调控机体紊乱的免疫应答,减轻炎症反应,目前已开展IgG4相关性疾病、类风湿关节炎、系统性红斑狼疮等疾病的临床探索。
2. 感染性疾病
针对病毒感染性疾病,γδT细胞可直接杀伤被病毒感染的细胞,抑制病毒复制,在慢性乙肝、丙肝、新冠病毒感染等疾病治疗中具备潜在应用价值。
3. 移植后排异与免疫重建
异体γδT细胞输注可在不引发GvHD的前提下,促进造血干细胞移植患者的免疫重建,预防移植后感染,降低肿瘤复发率。
国内γδT细胞临床研究最新进展(2026年)
目前国内γδT细胞治疗已形成药企IND注册临床+医院IIT研究者发起研究双轨并行的格局,多款创新疗法进入临床阶段,研发进度位居全球前列。
一、IND获批项目(NMPA默示许可,注册类临床)
1. 暨德康民 — γδ-T细胞注射液
适应症:晚期肝细胞癌
获批时间:2024年4月(国内首个获批的γδT细胞创新药IND)
临床进展:2026年3月30日在暨南大学附属第一医院启动多中心I期临床,登记号CTR20260344,计划入组26例,重点评估药物安全性、耐受性及II期推荐剂量,是全球首个针对实体瘤的异体γδT注册临床研究。
2. 清辉联诺 — QH104A(CAR-γδT)
靶点:B7-H3
适应症:复发/进展性中枢神经系统恶性肿瘤(脑胶质瘤等)
临床进展:登记号CTR20254427,I期临床,2025年12月完成首例患者给药,由北京天坛医院牵头,是全球首款靶向B7-H3的现货型CAR-γδT细胞疗法,成功突破血脑屏障,填补中枢神经系统肿瘤细胞治疗空白。
3.Acepodia — ACE1831(γδ2 T细胞)
适应症:IgG4相关性疾病(自身免疫病)
获批时间:2025年12月(中国IND获批)
临床进展:启动I/IIa期多中心临床研究,布局自身免疫性疾病领域,拓展γδT细胞非肿瘤适应症应用。
二、CAR-γδT创新管线临床研究
清辉联诺 QH103(CD19-CAR-γδT)
适应症为复发/难治性B细胞急性淋巴细胞白血病,临床登记号ChiCTR2400092462,处于I期临床探索阶段,针对血液肿瘤精准治疗。
广州医科大学附属第二医院 — 双靶点CAR-γδT
靶向GPC3/Mesothelin双靶点,针对肝癌等实体瘤开展I期临床研究,登记号NCT06196294,通过双靶点提升肿瘤识别精准度。
三、研究者发起IIT项目(医院主导,临床探索)
1. 血液肿瘤方向
华中科技大学同济医院(NCT07237230):异体γδT细胞输注预防高危急性髓系白血病移植后复发,2025年7月启动,招募中,计划入组40例;
苏州大学附属第一医院(NCT06696833):CD19靶向CAR-γδT细胞治疗复发/难治性B细胞急性淋巴细胞白血病,开展单臂、开放标签早期临床。
2. 实体瘤方向
上海市第十人民医院(NCT07204496):γδ-T细胞注射液治疗晚期膀胱癌IIT临床,评估安全性与初步抗肿瘤疗效;
中国人民解放军总医院(301医院)、空军军医大学西京医院等:开展γδT细胞联合PD-1抑制剂、干扰素治疗黑色素瘤、肺癌、肝癌等实体瘤,小样本临床数据显示疾病控制率达60%-80%,安全性良好。
产业转化关键支撑:华辰生物 γδT细胞上游核心解决方案
γδT细胞临床转化的核心瓶颈,在于高纯度、高扩增、高杀伤、临床级合规的细胞制备工艺。苏州华辰生物作为CGT全流程解决方案合作伙伴,推出临床级γδT细胞高效激活扩增体系,为IND申报、IIT研究、规模化现货型细胞药生产提供稳定可靠的上游原料与工艺方案。
1. 核心产品矩阵
novaT-36™ 无血清培养基:无动物源、化学成分限定、含重组白蛋白,同步支持Vδ1/Vδ2亚群生长,适配临床级应用。
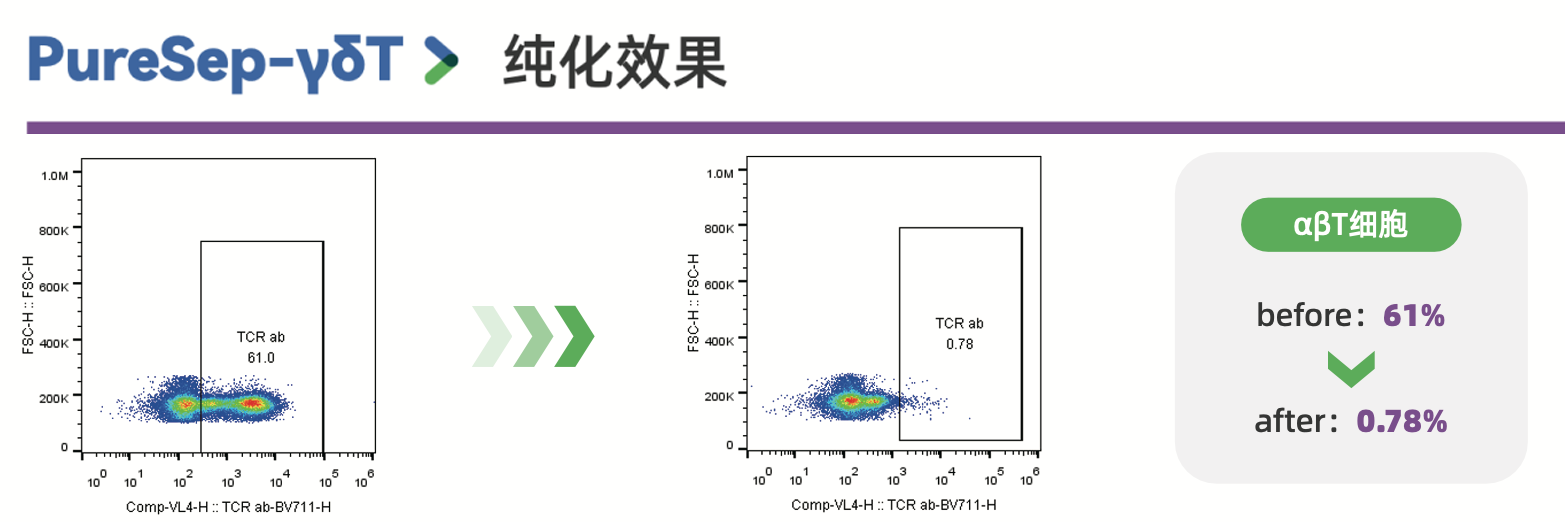
pureSep-γδT 纯化试剂:密度梯度负选高效去除αβT细胞,实现高纯度γδT富集,供者间稳定性强。
2. 第二代纯因子标准化扩增工艺
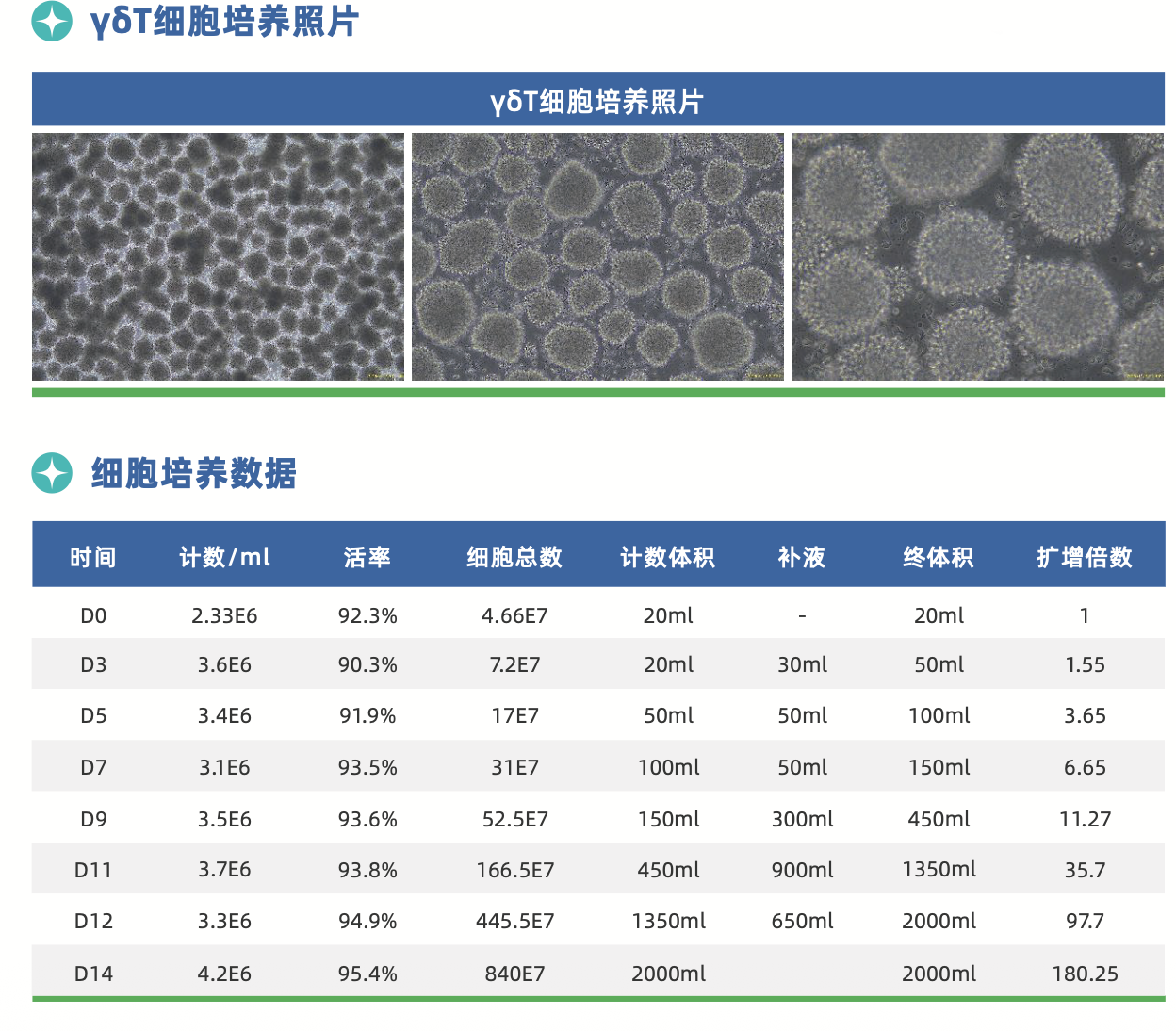
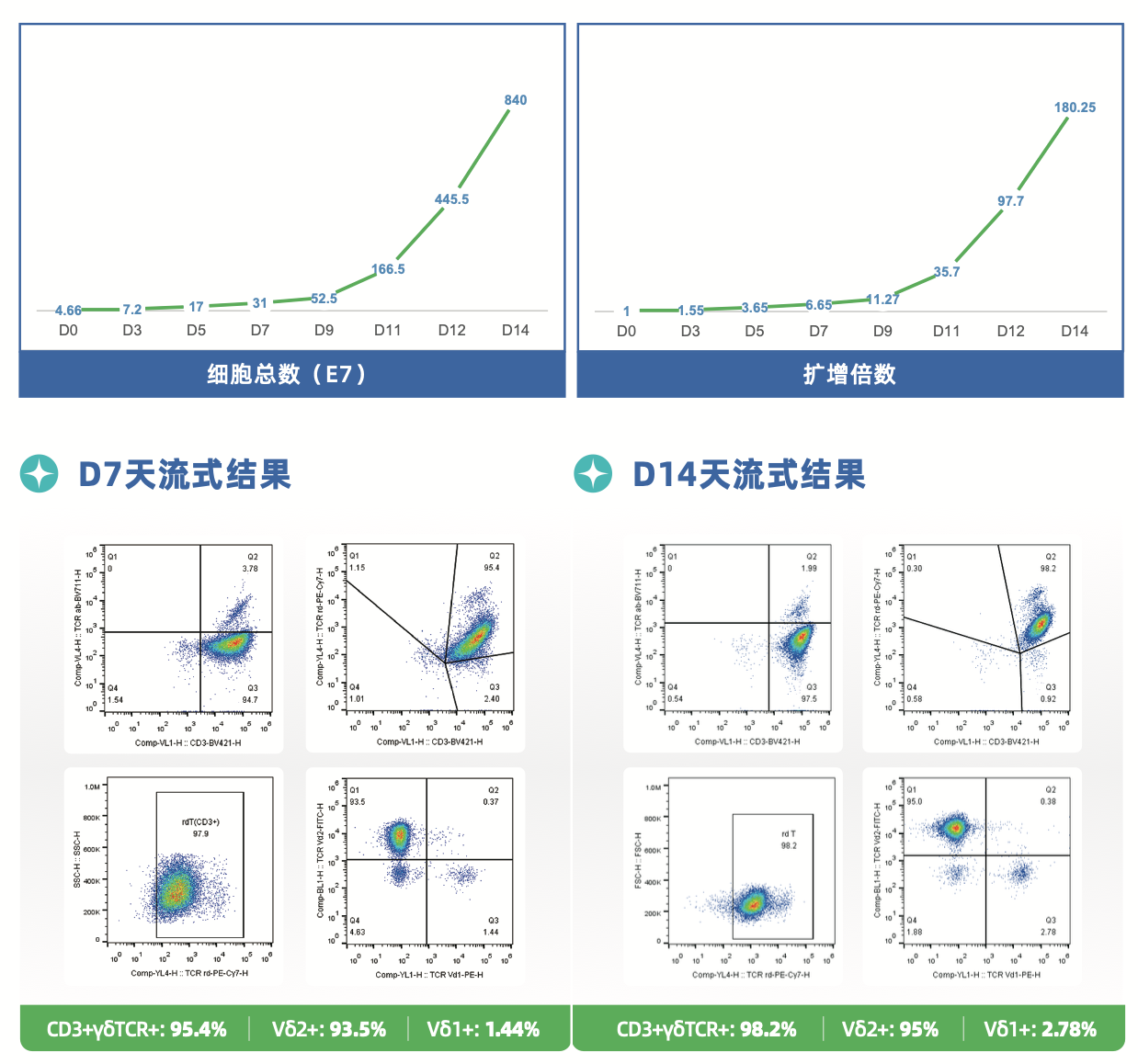
第二代(纯因子方案):预纯化+抗体激活,全程无化学刺激,D7纯度>90%,D14纯度>98%,满足异体临床级使用要求。
3. 核心性能数据
扩增:D14最高扩增242倍,细胞活率稳定>90%
纯度:D14流式 CD3+γδTCR+ >98%,满足异体使用标准
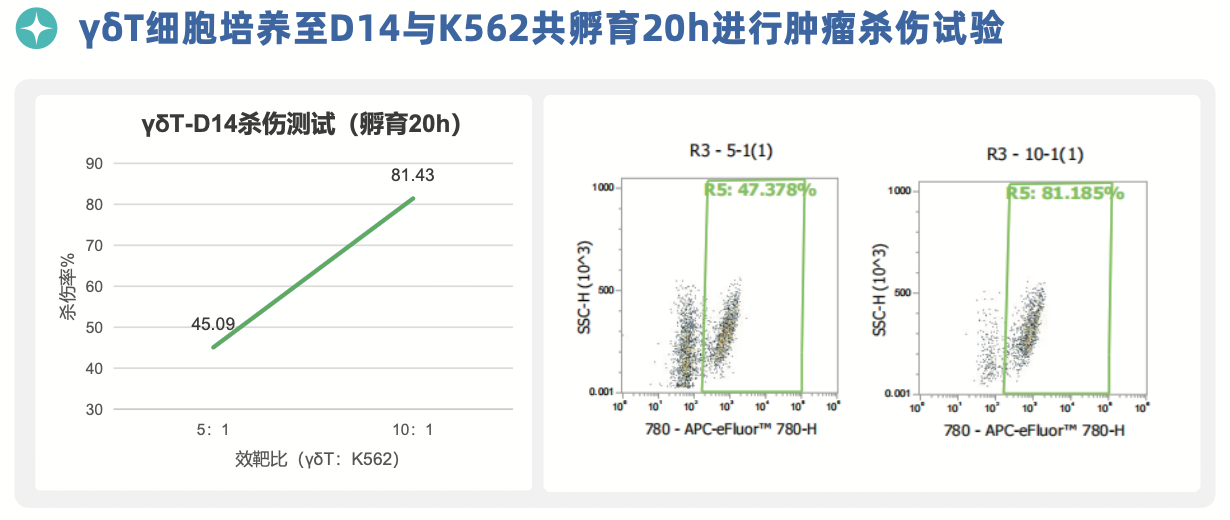
杀伤:对K562细胞20h杀伤率最高81.43%
优势:高增殖、高纯度、杀伤性强、合规可控、批间稳定
行业趋势与未来展望
2026年作为细胞治疗行业规范化发展的关键之年,随着新版《生物医学新技术临床研究和转化应用管理条例》落地,γδT细胞治疗的临床转化将进一步提速。
从技术发展来看,异体通用型γδT细胞是主流方向,CAR工程化修饰、双靶点改造、联合免疫治疗是技术升级核心;从适应症布局来看,实体瘤仍是研发重点,自身免疫性疾病、感染性疾病等蓝海领域逐步拓展;从产业化来看,国内γδT细胞疗法已进入临床数据读出关键期,2026-2027年将有更多临床数据公布,有望推动产品进入II/III期临床,加速商业化落地。
相较于传统CAR-T细胞,γδT细胞凭借现货通用、成本更低、实体瘤有效、安全性更高的优势,有望颠覆现有细胞治疗格局,成为下一代普惠型细胞治疗产品,中国也有望在全球γδT细胞治疗领域占据领先地位。
临床项目官方查询渠道
1. 国家药品监督管理局药物临床试验登记与信息公示平台:查询CTR开头注册类临床项目;
2. 中国临床试验注册中心(ChiCTR):查询国内IIT临床研究项目;
3. [ClinicalTrials.gov](ClinicalTrials.gov):查询国际注册NCT编号临床项目。
注:本文数据截至2026年4月,临床研究进展持续更新,最终以官方公示为准
返回顶部